将固体A置于密闭容器中.在一定温度下发生下列反应:①A,②2C.达到平衡时.c(D)=0.5mol•L
8.将固体A置于密闭容器中,在一定温度下发生下列反应:
①A(s)?B(g)+C(g);
②2C(g)?D(g)+E(g).
达到平衡时,c(D)=0.5mol•L-1,c(C)=4mol•L-1,则此温度下反应①的平衡常数为( )
分析 反应①的平衡常数k=c(B)•c(C),A分解生成的B为平衡时C与分解的C之和,由反应②可知分解的c(C)为平衡时c(D)的2倍,求出为A分解生成的B,代入反应①的平衡常数K=c(B)•c(C)计算.
解答 解:平衡时c(C)=4mol•L-1,c(D)=0.5mol•L-1,A分解生成的C的浓度为4+0.5×2=5mol•L-1,则:
所以A分解生成的B的浓度为5mol•L-1,
所以反应①的平衡常数k=c(B)•c(C)=5mol•L-1×4mol•L-1=20mol2•L-2.
故选:B.
点评 本题考查化学平衡常数的计算,解题关键在于平衡时C为A分解生成的C与分解的C之差,难度中等.
练习册系列答案
相关习题
科目:高中化学来源:题型:选择题
2.设 NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.7.8 gNa2O2含有的阴离子数目为 0.2NAB.56gFe 与稀 H N03 完全反应时一定转移3NA个电子C.1 molC10H22分子中共价键总数为 3lNAD.已知热化学方程式2SO2(g)+O2?(g)2SO(g) 3△=-QkJ/mol(Q>0),则将 2NA 个SO2分子和 NA 个O2分子置于一密闭容器中充分反应后放出QkJ的热量查看答案和解析>>
科目:高中化学来源:题型:解答题
3.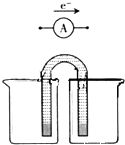 Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液.
(1)该电池的负极材料是Zn(或锌).电池工作时,电子流向正极(填“正极”或“负极”).
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀.欲除去Cu2+,最好选用下列试剂中的b(填代号).
a.NaOH b.Zn c.Fe d.NH3•H2O
(3)电池是应用广泛的能源.
设计两种类型的原电池,比较其能量转化效率.限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线.完成原电池甲的装置示意图如图),并作相应标注.要求:在同一烧杯中,电极与溶液含相同的金属元素.以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙.甲、乙两种原电池中乙的能量转化效率较低,其原因是甲可以保持电流稳定,化学能基本都转化为电能;而乙中的活泼金属还可以与CuSO4溶液发生置换反应,部分能量转化为热能.
查看答案和解析>>
科目:高中化学来源:题型:解答题
16.工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程.
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)$frac{underline{;;△;;}}{;}$Na2S2O3(aq) (Ⅲ)
(1)装置A中发生的化学反应方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为2:1.
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择c
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是控制滴加硫酸的速度.
(4)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是溶液变澄清(或混浊消失),装置E的作用为吸收SO2防止污染空气
(5)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:取少量产品溶于足量稀盐酸中,静置,取上层清液(或过滤后取滤液),滴加BaCl2溶液,若出现白色沉淀则说明含有Na2SO4杂质.
已知:Na2S2O3•5H2O遇酸易分解:S2O32?+2H+=S↓+SO2↑+H2O供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
查看答案和解析>>
科目:高中化学来源:题型:解答题
3.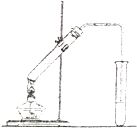 实验室中按照一定顺序混合2mL浓硫酸、3mL乙醇、2mL乙酸后加热制备乙酸乙酯,将产生的蒸汽经导管通到饱和碳酸钠溶液的液面上(如图所示).
实验室中按照一定顺序混合2mL浓硫酸、3mL乙醇、2mL乙酸后加热制备乙酸乙酯,将产生的蒸汽经导管通到饱和碳酸钠溶液的液面上(如图所示).
(1)为安全起见,药品混合必须按照一定顺序,先加3ml乙醇,后加2ml浓硫酸和2ml乙酸,通常为了防止爆沸,还需要往混合液中加入碎瓷片.
(2)上述制备乙酸乙酯的化学方程式为CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOC2H5+H2O,浓硫酸在反应中起的作用催化剂、吸水剂.
(3)上述方案中哪些措施利于生成更多的乙酸乙酯?将乙酸乙酯从试管中蒸出,用浓硫酸将反应产生的水吸收,多加乙醇
(4)右侧导管不能伸入到液面以下的原因是防止试管内液体倒吸入导管,实验过程中某同学观察到饱和碳酸钠溶液中有沉淀析出,该物质可以是碳酸氢钠,饱和碳酸钠溶液的作用是中和乙酸、溶解乙醇,降低乙酸乙酯的溶解度.
(5)实验结束后,为了得到纯净的乙酸乙酯,通常还需要用饱和食盐水、饱和氯化钙、水洗涤粗产品,然后分液,取上层液体,加入无水硫酸钠干燥,最后蒸馏得到精制乙酸乙酯.
查看答案和解析>>
科目:高中化学来源:题型:填空题
13.氨的合成是重要的一项化工生产.已知合成氨有关能量变化的图象如图1.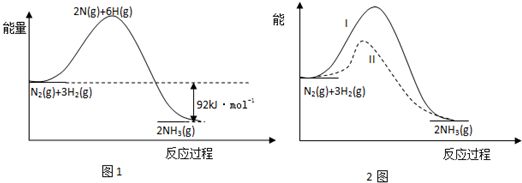
(1)反应 N2(g)+3H2(g)?2NH3(g)△H=-92KJ/mol;
(2)化学反应可视为旧健断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.现提供以下化学键的键能(kJ•mol-1):H-H:436,N≡N:946,则N-H的键能是
391kJ•mol-1;
(3)在一定条件下按图2实线I进行,改变某条件按图2虚线II进行,则该条件可能是加入催化剂;
(4)在一个密闭容器中加入1molN2、3mol H2,一定条件下充分反应,其热效应始终小于92kJ,请说明原因可逆反应不能完全转化;
(5)在一个密闭容器中加入amolN2、bmol H2,达到平衡时n(N2):n(H2)=1:3,则a:b=1:3.
(6)在一个5L密闭容器中加入8molN2、22mol H2,2min内v(N2)=0.2mol•L-1•min-1,5min后达化学平衡,维持温度不变平衡时压强是反应前的11/15.2min和平衡时n(NH3)分别是4mol和8mol.(写出此结果的计算过程)
查看答案和解析>>
科目:高中化学来源:题型:选择题
20.下列表示物质结构的化学用语或模型图正确的是( )
A.H2O的结构式:H-O-HB.乙烯的结构简式为CH2CH2C.CO2的比例模型: D.丙烯的电子式:
D.丙烯的电子式:查看答案和解析>>
科目:高中化学来源:题型:多选题
18.在约100℃的温度下,NaCl稀溶液中[H+]为1×10-6 mol•L-1.下列说法中正确的是( )
A.该NaCl溶液显酸性B.该NaCl溶液显中性C.该NaCl溶液中KW=1×10-14 mol2•L-2D.该NaCl溶液中KW=1×10-12 mol2•L-2查看答案和解析>>
相关知识
在某一容积为2 L的密闭容器内,加入2 mol的CO和2 mol的H2O,高温加热,发生如下反应:CO(g) +H2O(g) CO2(g) + H2(g);1molCO完全反应放热a kJ。反应达到平衡后,测得
碳汇是指通过植树造林、植被恢复等措施,利用植物光合作用吸收大气中的二氧化碳,从而减少温室气体在大气中浓度的过程、活动或机制。已知利用植物的光合作用每吸收1mol
将气体A,B置于容积为2L的密闭容器中,发生反应:4A(g)+B(g)=2C(g
温度压强一定,在催化剂铁触媒作用下,向一密闭容器充入N2、H2和NH3.若起始时n(N2)=x mol、n(H2)=y mol、n(NH3)=z mol (x、y、z均不为0 ),平衡时n(N2)=0.1mol、n(H2)=0.3mol、n
对于可逆反应:2A(g)+3B(g)===3C(g),在一定条件下,使一定量A和B反应达到平衡状态时,具有的性质是 ( )A.各物质浓度比为c(A):c(C)=“2”:3:3B.在温
在温度TK下,反应CaCO3(s)=CaO(s)+CO2(g)的平衡系统的压...
[题目]欲测量久置在空气中的NaOH固体中Na2CO3的质量分数.取a g样品.按下列方案进行实验.合理的是A.与足量稀盐酸充分反应.用排水法收集到V mL气体B.与足量稀盐酸充分反应.称量反应后的溶液.质量为m1 gC.与足量Ca(OH)2溶液充分反应.将沉淀过滤.洗涤.干燥.得到m2 g固体D.与足量浓盐酸充分反应.逸出的气体用NaOH� 题目和参考答案——青夏教育精英家教网——
C中 . .D中 .(2)用化学方程式表示图中所体现的化学反应 .(3)以上变化的反应类型是 . Al3+ . SO42
(1)某银白色固体A在空气中点燃.火焰呈黄色.并生成淡黄色固体B,将A在空气中露置.最后变成白色固体C.将A.B投入水中都生成D.则A是Na,B是Na2O2,C是Na2O,D是NaOH.B与H2O反应的离子方程式为2Na2O2+2H2O=4Na++4OH
用菊花的茎尖进行植物组织培养可培育出试管苗.下面关于这一过程的说法正确的是( )A.进行培养时.一次性加足营养物质以防止污染B.整个培养过程应在光下进行.有利于长叶C.要根据培养过程的实际情况.更换培养基D.整个培养过程都应在密闭条件下进行.以免杂菌的污染 题目和参考答案——青夏教育精英家教网——
网址: 将固体A置于密闭容器中.在一定温度下发生下列反应:①A,②2C.达到平衡时.c(D)=0.5mol•L https://m.huajiangbk.com/newsview631171.html
| 上一篇: 一种具有生产负离子功能的磁性塑料 |
下一篇: 环保板材释放6000负离子,竟便 |