用于细胞治疗制造的微流体装置中高通量 CRISPR/Cas9 介导的原代人类 T 细胞基因编辑,Advanced Materials Technologies
用于细胞治疗制造的微流体装置中高通量 CRISPR/Cas9 介导的原代人类 T 细胞基因编辑
Advanced Materials Technologies ( IF 6.4 ) Pub Date : 2023-05-04 , DOI: 10.1002/admt.202300275
Michaela Welch 1 , Deborah A. Flusberg 1 , Peter Hsi 1 , Nerses J. Haroutunian 1 , Jose A. Santos 1 , Ernest S. Kim 1 , Stacey Markovic 1 , Jonathan R. Coppeta 1 , Charles A. Lissandrello 1 , Jenna L. Balestrini 1 , Vishal Tandon 1
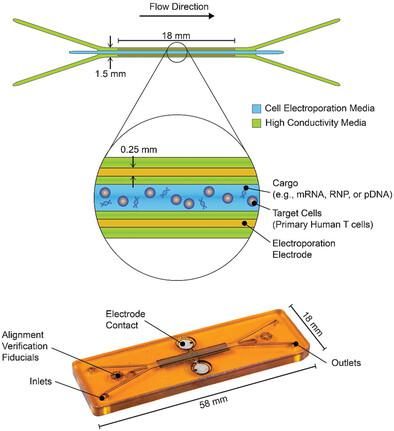
自体细胞疗法在治疗血液癌症方面非常成功,并且具有用于多种适应症的潜力。快速且低成本地制造这些疗法仍然是一个重大挑战。细胞疗法生产的一个关键瓶颈是靶细胞的基因修饰,这通常是使用病毒载体完成的。由于载体的开发和生产成本昂贵,因此使用电穿孔的非病毒基因转移正在成为下一代疗法的首选转染方法。然而,大多数商业电穿孔系统都是为研究用途而不是大规模临床制造而构建的。这里介绍的微流控连续流电穿孔装置具有多种优点,包括大规模和高通量处理、高性能、以及自动化的潜力。它使用 Cas9 引导的核糖核酸 (RNA) 核糖核蛋白复合物 (RNP) 和信使 RNA (mRNA) 转染原代人类 T 细胞,效率高达 99-100%,且对活力的影响极小。此外,经过初步优化研究,该装置转染3.5 kbp质粒脱氧核糖核酸的效率高达86%。单个微通道每小时可提供高达 96 亿个细胞的总处理吞吐量。高通量和高性能的结合实现了未来“现成”同种异体细胞疗法所需的处理规模。该装置经初步优化研究,转染3.5 kbp质粒脱氧核糖核酸的效率高达86%。单个微通道每小时可提供高达 96 亿个细胞的总处理吞吐量。高通量和高性能的结合实现了未来“现成”同种异体细胞疗法所需的处理规模。该装置经初步优化研究,转染3.5 kbp质粒脱氧核糖核酸的效率高达86%。单个微通道每小时可提供高达 96 亿个细胞的总处理吞吐量。高通量和高性能的结合实现了未来“现成”同种异体细胞疗法所需的处理规模。
"点击查看英文标题和摘要"
更新日期:2023-05-04
相关知识
CRISPR/Cas9 technology in disease research and therapy: a review
CRISPR基因编辑创造永不凋谢的牵牛花,只需敲除ACO1基因
CRISPR/Cas9基因编辑技术在家畜育种新材料创制中的研究进展
用于西兰花和亚细胞定位的高效遗传转化系统,Frontiers in Plant Science
Progress of the Application of CRISPR/Cas9 Gene Editing Technology in Pig Breeding
玩儿转“基因编辑”
Target Improvement of Rice Based on CRISPR/Cas9 Gene Editing Technology
基于CRISPR的月季RcTCP基因编辑技术研究
细胞保护剂的使用方法是什么?
DeepTech发布生命科学十大技术趋势,基因编辑在列
网址: 用于细胞治疗制造的微流体装置中高通量 CRISPR/Cas9 介导的原代人类 T 细胞基因编辑,Advanced Materials Technologies https://m.huajiangbk.com/newsview531102.html
| 上一篇: 绿原酸和咖啡酸的体外和体内抗氧化 |
下一篇: 育种4.0:基因编辑设计中国种子 |